Ânodo vs. Cátodo: Qual é Positivo e Negativo?
No campo da eletroquímica e dos circuitos elétricos, a terminologia de “ânodo” e “cátodo” tem uma importância significativa. Essas duas variedades distintas de eletrodos assumem funções críticas em uma variedade de sistemas diversos, desde baterias rudimentares até aplicações tecnológicas de ponta.
Permita-nos aprofundar a análise das disparidades que envolvem essas distinções, incluindo uma avaliação de suas respectivas conotações positivas e negativas, ao mesmo tempo em que fornece uma compreensão clara de como discernir se elas são caracterizadas como favoráveis ou desfavoráveis.
O que é um eletrodo?
Um eletrodo pode ser conceituado como uma substância que facilita a transmissão de carga elétrica dentro de um ambiente não metálico. Sua função consiste em permitir o fluxo de corrente elétrica para dentro ou para fora de um sistema, como uma solução eletrolítica. Antes de aprofundar as características específicas de um cátodo ou de um ânodo, é essencial compreender esse entendimento fundamental de um eletrodo e seu papel na condução de eletricidade.
Em essência, um eletrodo funciona como um meio para estabelecer comunicação elétrica entre um elemento não metálico dentro de um circuito e outra entidade condutora.
O que é um ânodo?

A designação de um eletrodo como ânodo ou cátodo depende da configuração específica do circuito elétrico no qual ele opera. Um ânodo é caracterizado pela ocorrência de oxidação, que resulta na perda de elétrons. Em uma célula galvânica, por exemplo, que transforma energia química em elétrica, como uma bateria em processo de descarga, o ânodo serve como terminal carregado negativamente porque, durante a oxidação, os elétrons são liberados no eletrodo e fluem pelo circuito externo.
Em contraste com os processos catódicos, como a corrosão, em que os elétrons fluem do ânodo para o cátodo, a eletrólise envolve uma corrente elétrica que faz com que os elétrons se movam na direção oposta, com o ânodo se tornando o eletrodo carregado positivamente.
O que é um cátodo?
 Crédito da imagem: Raspberry Pi
Crédito da imagem: Raspberry Pi
O cátodo funciona como o local para a transferência de elétrons, permitindo a perda de elétrons. Dentro de uma célula galvânica, cumpre o papel do eletrodo carregado positivamente devido ao processo de redução iônica em que as partículas perdem sua carga ao aceitar elétrons da superfície do eletrodo e posteriormente aderir a ele na forma de um precipitado.
Em contraste, durante a eletrólise, o cátodo funciona como o pólo carregado negativamente e, assim, atrai os íons carregados positivamente presentes na solução eletrolítica.
Ânodo vs. Cátodo: Clarificando a Polaridade
No passado, pensava-se inicialmente que a eletricidade fluía do positivo para o negativo, o que na verdade é o inverso do que atualmente compreendemos ser preciso. Como resultado desse mal-entendido inicial, alguns indivíduos passaram a associar o ânodo à negatividade e o cátodo à positividade.
Para determinar com precisão se um determinado eletrodo constitui um ânodo ou cátodo dentro de uma configuração de circuito elétrico específico, é essencial compreender as respectivas funções dos processos de oxidação e redução que ocorrem em cada eletrodo. A designação do ânodo ou do cátodo para um determinado eletrodo dependerá da natureza do circuito que está sendo considerado.
O que é um eletrólito em uma bateria?
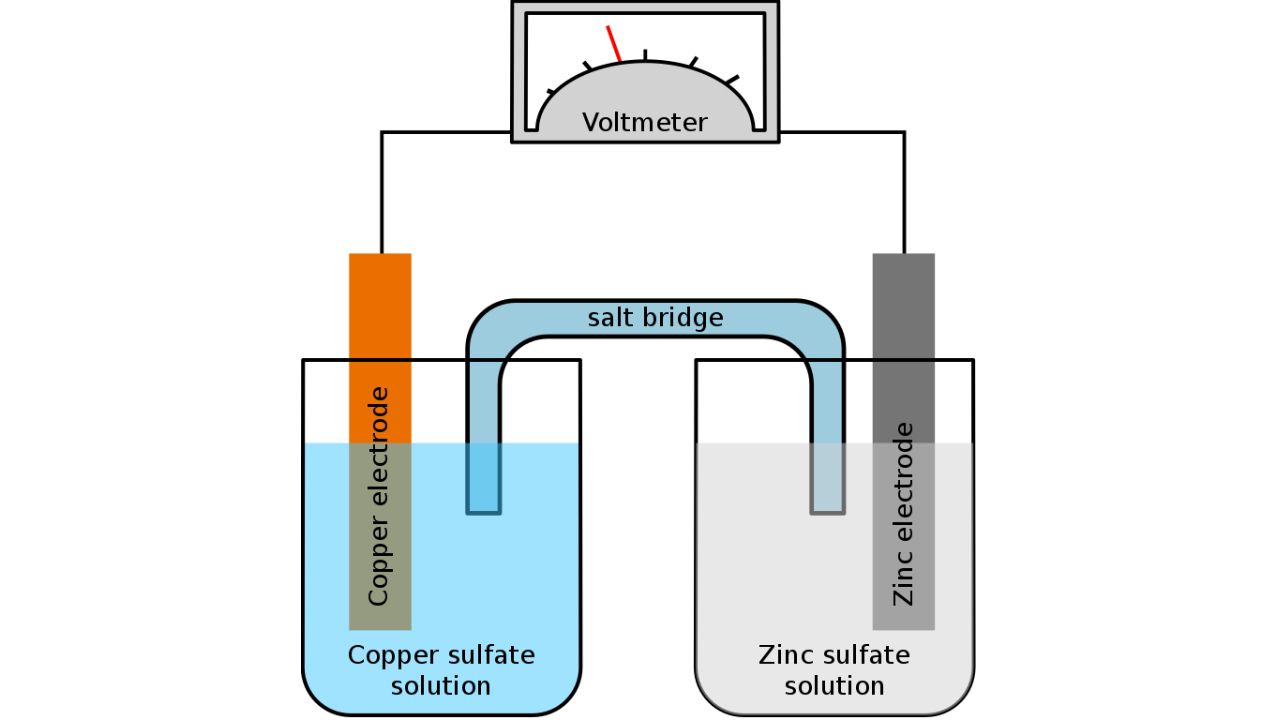 Crédito da imagem: Tinux/gringer/Wikimedia Commons
Crédito da imagem: Tinux/gringer/Wikimedia Commons
O eletrólito em uma bateria serve como um meio condutor que facilita a transferência de íons entre o ânodo e o cátodo, mantendo sua neutralidade elétrica. Essa migração iônica é crucial para as reações químicas que ocorrem durante os ciclos de carga/descarga. Para entender melhor este tópico, consulte
Qual deles é positivo?
Para compreender as polaridades associadas aos eletrodos dentro de uma célula ou circuito elétrico, é essencial contemplar os processos duais que ocorrem em cada local. Ao se tratar de uma célula galvânica, o ânodo sofre oxidação e assume o papel de eletrodo carregado negativamente. Por outro lado, durante a eletrólise, o mesmo ânodo se transforma no eletrodo carregado positivamente. Inversamente, o cátodo que promove a redução assume a função de eletrodo carregado positivamente em uma célula galvânica. No entanto, no contexto da eletrólise, esse mesmo cátodo serve como terminal carregado negativamente.